3F poursuit son expansion en Amérique Latine avec la création d’une nouvelle entité en Équateur. La société, basée à Quito, va proposer directement l’ensemble de notre gamme de produits, mais aussi des véhicules – camions, ambulances et pick-up – pour les pompiers fabriqués localement.
Cette création renforce la position de 3F sur le continent américain avec une présence élargie au Mexique, au Panama et à l’ Equateur.
Actualités
3F ÉQUATEUR
SHG lance une nouvelle pompe compacte : ALPSEE
SHG a le plaisir de vous présenter la pompe submersible ALPSEE, le dernier-né de sa gamme. Conforme à la norme DIN 14425, ALPSEE séduit notamment par son dispositif d’aspiration plat intégré, permettant un pompage automatique en eaux peu profondes (quelques millimètres seulement) sans accessoires supplémentaires. Pour une utilisation optimale et sans effort, des kits d’accessoires comprenant un clapet anti-retour et un tuyau spiralé en PVC de 3 ou 5 m sont également disponibles. Compacte et économique, ALPSEE est à découvrir dans sa fiche technique.
Les voitures électriques : un défi pour les pompiers
Les voitures électriques sont de plus en plus nombreuses sur nos routes. Si elles présentent certains avantages écologiques, elles représentent un nouveau défi pour las pompiers. Les batteries au lithium peuvent brûler et réagissent avec l’eau et la mousse en libérant des gaz toxiques et inflammables à très haute température. La poudre n’est pas efficace.
Pour contrôler ce risque, 3F propose une gamme de couvertures spéciales anti-feu TEXCAR, disponible en 4 dimensions. TEXCAR résiste aux hautes températures et évite la concentration des gaz susceptibles d’exploser.
En savoir plus…
VdS certifie FREEGEN ULTRA
FREEGEN ULTRA a été certifié selon le nouveau référentiel normatif VdS 3124 :2025-01 pour l’extinction en systèmes sprinkler. Cela a été réalisé conjointement avec notre partenaire TSF Allemagne.
Notre produit a passé avec succès tous les essais d’extinction sur feux d’une longue liste de solvants et d’hydrocarbures, à la concentration d’emploi de 3%. La liste inclut un des solvants les plus difficiles à éteindre, l’aldéhyde, qui a été éteint au taux d’application de 25 l/m2.mn
De plus, FREEGEN ULTRA au taux de 1% a été approuvé sur feux de plastiques.
Les essais confirment l’efficacité de FREEGEN ULTRA employé dans les conditions les plus difficiles.
SCORPE Days : un évènement à ne pas manquer
3F a participé à l’évènement organisée par SCORPE sur son site en France les 17 et 18 juin 2025. Plus de 40 distributeurs venus d’Europe, d’Asie et d’Amérique latine ont assisté à une démonstration de grande ampleur mettant en action les dernières innovations des équipements de secours : outils d‘extraction, ventilateurs, équipements de recherche de victimes, lumières,… Tout cela réalisé sur le terrain d’exercice de TCS, l’école de SCORPE pour les pompiers. Nous avons vu la capacité d’extinction impressionnante du FAS sur un feu de van rempli de 12 pneus, éteint avec seulement 220 litres d’eau et additif FREEFOR SF. Il y a eu aussi l’opportunité de voir le robot high-tech TEC-800 de ANGATEC.
Journées Thématiques à Troyes – France du 19 au 21 Mars 2025
La revue SOLDATS DU FEU a organisé du 19 au 21 mars 2025 les Journées Thématiques. Plus de 100 délégués participaient à l’évènement. 3F était présent sur le stand de son distributeur JCM pour ses émulseurs sans fluor et additifs pour feux de classe A.
Un des thèmes abordés a été les nouveaux émulseurs sans fluor dits F3. Le Dr. Thierry Bluteau, expert chimiste de LEIA Ltd, est revenu sur les problèmes rencontrés avec les F3, comme la viscosité ‘’trop’’ élevée, l’instabilité au stockage et la sensibilité à l’eau. Il a évoqué les solutions apportées par les fabricants innovants, tel 3F. L’évènement a été un franc succès et a confirmé le mouvement de la profession vers des produits performants et respectueux de l’environnement.
Des AFFF aux F3 : les F3 sont créés — Partie 6
Dans les articles précédents (partie 1 à 5) nous avons traité l’Histoire, la Chimie, L’Impact sur la Santé et l’Environnement et la Réglementation pour les produits contenant des PFCs.
Introduction
Depuis le retrait de 3m de la chimie du fluor en 2000 jusqu’au marché actuel, un nombre croissant de fabricants ont présenté des émulseurs sans fluor. Si aujourd’hui, les fabricants disent que les F3 sont une évidence voire une obligation, cela n’a pas été toujours le cas depuis les années 2000 !
Les premières années 2000-2012
En réalité, pendant plus de 12 ans, seulement 2 chimistes – nommés Ted Shaeffer et Thierry Bluteau -, se sont réellement intéressés et ont travaillé pour proposer la première génération de F3, respectivement RE-Healing Foam (Solberg) et ECOPOL (BIO-EX). Ces premiers F3 étaient très performants sur feux de solvants polaires, mais présentaient des faiblesses sur les feux d’hydrocarbures.
Pendant ces années, la bataille faisait rage entre ces deux sociétés pionnières et leurs concurrents – regroupés sous la bannière FFFC – à propos de maintien ou pas de la technologie AFFF sur le marché. Malgré tous leurs efforts pour miner la technologie F3, le changement était en marche et de nombreux utilisateurs avaient décidé de changer pour un émulseur ‘’vert’’ et efficace.
Les dernières années 2012-2024
Cette période peut être considérée comme une transition, quand il est devenu indéniable que les F3 deviendraient les émulseurs du futur et les AFFF des produits du passé. Cette période a éveillé la conscience des utilisateurs et des fabricants et en quelques années la deuxième génération des F3. La principale avancée est la performance améliorée sur feux d’hydrocarbures, les produits annonçaient des performances maximales selon les normes EN 1568-3 et UL162. Les chimistes ont changé : Thierry Bluteau est conseil auprès de 3FFF Ltd et Ted Shaeffer est à la retraite. D’autres chimistes se sont attelés à la création des F3.
La technologie F3
Le chimiste a dû résoudre un problème de taille : le retarit de la formule des molécules perfluorées a signifié la nécessité d’utiliser une composé/mélange chimique combinant des propriétés extinctrices similaires, à savoir la résistance à la chaleur et à la contamination par le carburant.
Nous avons vu dans les articles précédents que les formules synthétiques sont basées sur l’association de tensio-actifs, de solvants et de polymères. Le choix est vaste pour le chimiste.
– Plus de 7000 tensio-actifs sont répertoriés
– Nous comptons entre 800 et 1000 solvants hydrophiles
– Pour les polymères, le choix est immense, probablement plus de 1000 classes de polymères existent, sans compter les nombreux copolymères et les variations de longueur et de ramification.
Il est possible d’apprécier la difficulté pour le chimiste à sélectionner parmi tous ces produits pour aboutir au produit final.
La formule adéquate pour un émulseur est l’équilibre entre les différents composants pour obtenir une performance extinctrice satisfaisante, tout en maintenant des caractéristiques satisfaisantes, telles que la densité, le pH, la viscosité, le foisonnement, le temps de décantation et la stabilité au vieillissement.
Hélas, l’emploi en excès de polymères entraine une augmentation importante de la viscosité, ce qui rend certains émulseurs impossibles à doser avec des proportionneurs classiques. Certains fabricants de doseurs ont dû modifier leur système d’injection pour prendre en compte cette viscosité élevée ; et dans certains cas, certains émulseurs ont juste impossibles à utiliser dans la pratique.
Nous avons vu que, même si les meilleurs F3 sont comparables en performance aux AFF, ils sont très visqueux et nécessitent l’emploi de doseurs spécifiques – et coûteux. Cela entraine un cout annexe imprévu qui en final augmente l’ensemble de l’équipement anti-incendie.
En dehors de la viscosité qui est un problème majeur, la majorité des F3 contiennent des quantités élevées de solvants – principalement des glycols et éthers de glycols – aux effets toxiques potentiels. Ces solvants migrent et pénètrent la peau, ce qui provoque des risques d’allergie, d’irritation/sensibilité cutanée, et d’autres effets sur la santé une fois dans le sang.
La troisième génération des F3
La société 3F s’est consacrée depuis ses débuts à proposer des produits F3 conçus pour répondre parfaitement aux besoins de l’utilisateur. Cette philosophie est ancrée dans son génome, 3F offre une gamme complète de F3 – sous la marque FREEGEN – pour répondre aux besoins du marché.
C’est pourquoi 3F a développé une technique exclusive et offre les émulseurs SMART FOAM ® ; cette technologie permet d’éliminer complètement les solvants de la formulation. De plus, 3F a mis au point une combinaison permettant de contrôler la viscosité finale de l’émulseur tout en maintenant un haut niveau de performance sur feux. C’est ainsi que 3F propose 2 SMART FOAM FREEGEN SF-LV et FREEGEN ULTRA utilisables avec tous les doseurs du marché – même avec un simple doseur de type Venturi.
CONCLUSION
La technologie F3 est facilement disponible et a démontré son efficacité. Grâce au support de la réglementation, l’industrie est déjà en cours de remplacement du stock d’AFFF par des F3. Les F3 sont en cours de développement pour offrir encore plus de possibilité, en termes de concentration d’emploi, foisonnement, efficacité, etc… Au moment du choix, le décideur et/ou chef des pompiers doit vérifier que l’émulseur est compatible avec ses besoins et son matériel, et répond aux critères de performances exigés (LastFire, VDS, EN, OACI,…)
Des AFFF aux F3 : Réglementation et pressions législatives — Partie 5
Les articles précédents (parties 1 à 4) ont traité de l’histoire, de la chimie, des impacts environnementaux et sanitaires de l’exposition aux PFAS.
Introduction
Les régulateurs sont de plus en plus conscients des risques impliqués par la fabrication et l’utilisation de composés perfluorés dans les produits industriels et de consommation et, par conséquent, de nombreux pays ont promulgué une législation restreignant l’utilisation et l’élimination des PFAS.
Le manque de connaissance des meilleures pratiques disponibles (BAP) ou de la loi ne constitue pas un moyen de défense lorsqu’il s’agit de défendre des actions susceptibles d’avoir conduit à une contamination de l’environnement, comme le résume la phrase juridique « ignorantia legis neminem excusat ‘’ (l’ignorance de la loi n’excuse personne). Cette doctrine apparaît pour la première fois dans la Bible dans Lévitique 5 : 17 : « Si quelqu’un pèche et fait ce qui est interdit dans l’un des commandements du Seigneur, même s’il ne le sait pas, il est coupable et sera tenu responsable. »
Une interprétation moderne de ce principe a été établie dans le cadre de la Convention de Rio en 1992, comme le principe de précaution selon lequel l’absence de preuves ne doit pas être considérée comme une preuve de l’absence de préjudice, en particulier lorsque des effets intergénérationnels à long terme peuvent être suspectés.
Les séminaires REEBOK
Peu de temps après l’annonce par la société 3M en mai 2000 de son retrait de la chimie à base de PFOS, RAK et ses collègues ont organisé une série de conférences internationales à Manchester et à Bolton pour discuter des problèmes environnementaux associés aux mousses anti-incendie. Ces séminaires Reebok, qui ont eu lieu en 2002, 2004, 2007, 2009 et 2013, ont attiré un grand nombre de représentants de l’industrie des produits fluorés, des régulateurs, des fabricants de mousse et des utilisateurs finaux tels que les services d’incendie du monde entier. Ces séminaires sont devenus le forum de facto de l’industrie pour discuter de l’élimination progressive des AFFF de classe B et de la transition vers les mousses sans fluor de classe B (F3).
Lors du premier séminaire Reebok en 2002, il a été souligné que la réglementation britannique sur les eaux souterraines de 1998 interdisait déjà le rejet de produits chimiques fluorés présents dans les mousses AFFF dans les eaux souterraines s’ils étaient PBT – persistants, bioaccumulables et toxiques. Malheureusement, étant donné le manque évident de connaissance de la signification du terme « organohalogéné » dans le règlement (SI 2746/1998), il a été dit que celui-ci n’était pas pertinent.
Les séminaires Reebok ultérieurs, en particulier en 2004 et 2007, se sont concentrés non seulement sur le PFOS, mais également sur le PFOA et les substances apparentées qui pourraient se dégrader en PFOA, un produit final typique de dégradation des PFCA perfluorés extrêmement persistants. La possibilité que des dérivés tels que le 8 :2FTS, tels que ceux trouvés dans les mousses de fluorotélomères C6/C8, se biodégradent pour produire du PFOA a d’abord été vigoureusement niée par l’industrie fluorochimique face aux preuves publiées suggérant le contraire. Cependant, la teneur entière de la discussion a changé à la suite des pressions exercées par l’EPA des États-Unis, qui ont abouti au programme de gestion du PFOA 2010-2015, qui a finalement abouti à l’exigence que les produits fluorotélomères contiennent moins de 25 ppb de PFOA ou de ses précurseurs.
i) 1998 : Sous réserve de l’alinéa (2) ci-dessous, une substance est dans la liste I si elle appartient à l’une des familles ou groupes de substances suivants :
a) les composés organohalogènes et les substances susceptibles de former de tels composés dans le milieu aquatique ;
ii) 2009 : Cela inclut notamment les éléments suivants lorsqu’ils sont toxiques, persistants et susceptibles de bioaccumulation :
a) les composés organohalogénés et les substances susceptibles de former de tels composés dans le milieu aquatique ;
UBA
La Commission de biosurveillance humaine de l’Agence fédérale allemande de l’environnement (das Umweltbundesamt ou UBA) a établi des niveaux déclencheurs pour le PFOS et le PFOA dans le plasma sanguin humain. La valeur HBM-I est la concentration plasmatique en ng/l (ppb) qui, selon les estimations, ne présente aucun risque appréciable pour la population humaine en cas d’exposition prolongée et, par conséquent, ne nécessite aucune mesure supplémentaire. Les concentrations entre HBM-I et HBM-II indiquent que les impacts sur la santé ne peuvent être exclus avec suffisamment de certitude et qu’une enquête plus approfondie est nécessaire avec l’introduction de mesures pour éliminer, réduire ou contrôler l’exposition, y compris l’identification des sources potentielles et la vérification des résultats d’analyse. Les concentrations plasmatiques supérieures aux valeurs HBM-II, indiquant des impacts possibles sur la santé, nécessitent une intervention immédiate pour réduire ou éliminer l’exposition et une évaluation de tout impact sur la santé.
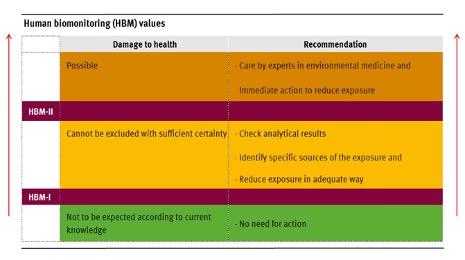
Les valeurs HBM-I et HBM-II pour le PFOS et le PFOA sont indiquées ci-dessous. Pour les femmes en âge de procréer, les valeurs HBM-II recommandées sont la moitié de celles de la population générale. Il convient de noter que les valeurs du PFOA sont inférieures à celles du PFOS.

Exposition des pompiers
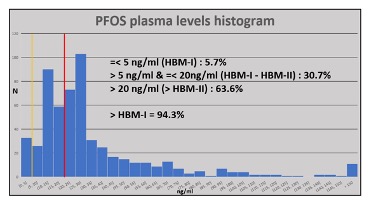
L’histoire des pompiers qui sont ou ont été professionnellement exposés aux AFFF à base de PFAS est une histoire assez différente. Les pompiers de longue date ainsi que ceux employés plus récemment peuvent avoir des taux plasmatiques bien supérieurs aux valeurs acceptables, en particulier pour le PFOS et son homologue PFHxS, qui sont corrélés. À titre d’exemple, la figure ci-dessous montre les niveaux plasmatiques de PFOS en 2015-2016 pour une vaste cohorte de pompiers d’une grande brigade de pompiers australienne, dans laquelle la majorité avaient des niveaux supérieurs au HBM-II. LE niveau HBM-I est indiqué par la ligne verticale jaune, HBM-II en rouge. Près des 2/3 de la cohorte échantillonnée dépassaient le HBM-II, ce qui indique un risque potentiel pour la santé.
La principale voie d’exposition des pompiers aux PFAS est clairement l’utilisation de mousse anti-incendie contenant des produits chimiques fluorés AFFF, que ce soit lors des opérations ou pendant la formation et la maintenance. Le mécanisme d’exposition est sans aucun doute soit l’inhalation d’aérosols moussants, en particulier pour le personnel ne portant pas d’appareil respiratoire autonome (ARI), soit l’absorption cutanée suite à l’immersion dans un aérosol de mousse. Lors de tout incident majeur impliquant de la mousse, par exemple un incendie dans un réservoir de carburant, environ un tiers de la mousse appliquée par les canons n’atteint jamais l’incendie lui-même mais est perdu sous forme de rideau de mousse et d’aérosol qui contamine la zone environnante et tout le personnel présent..

Eau potable
L’eau potable est la seule voie d’exposition inévitable pour tout le monde. L’apport moyen est calculé à environ 2 litres/jour au cours de la vie. Les apports hebdomadaires totaux maximaux (DHT) sont calculés sur cette base.
La directive révisée de l’UE sur l’eau potable est entrée en vigueur en janvier 2021, avec une conformité totale le 12 janvier 2023, et comprend des mesures visant à lutter contre les contaminants émergents tels que les perturbateurs endocriniens et les PFAS, ainsi que les microplastiques. La concentration maximale de tous les composés PFAS combinés est de 0,5 μg par litre d’eau (500 ppb). Alternativement, les États membres peuvent surveiller la somme de 20 composés PFAS spécifiés, pour lesquels le maximum est de 0,1 μg/l (100 ppb).
L’Institut national néerlandais pour la santé publique et l’environnement (RVIM) a récemment déterminé de nouvelles limites de risque pour les PFAS dans les eaux de surface [*2022-0074 RVIM 2022-09-08] sur la base des valeurs sanitaires dérivées de l’EFSA pour les PFAS en 2020. Les nouvelles limites de risque sont de 0,3 ng/l (0,3 ppt) pour le PFOA, de 7 pg/l (0,007 ppt) pour le PFOS et de 10 ng/l (10 ppt) pour le Gen-X. Celles-ci sont bien inférieures aux normes actuelles pour ces PFAS.
Produits alimentaires
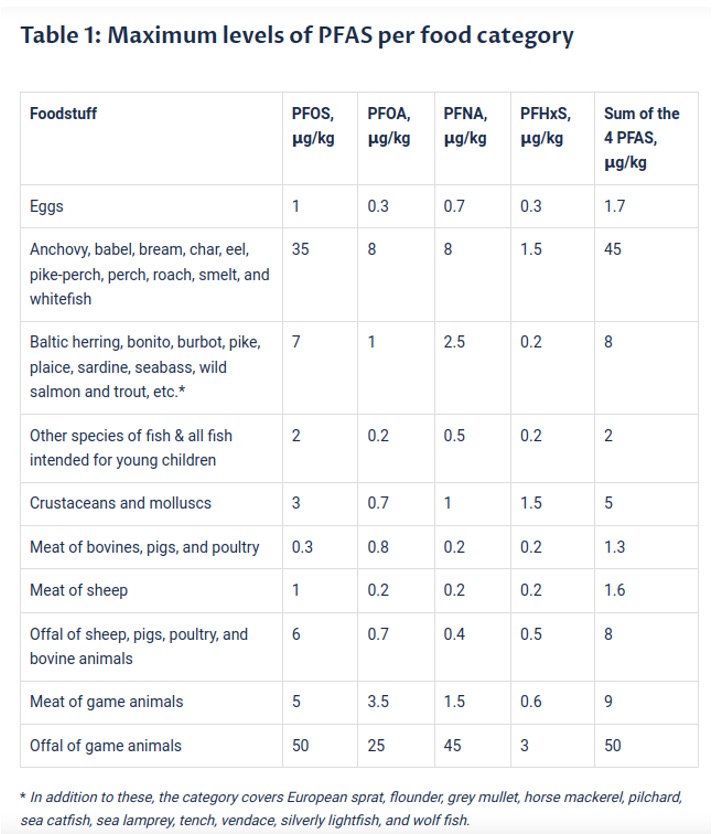
Les limites des PFAS dans certains produits alimentaires sur le marché de l’UE sont répertoriées dans le tableau 1. Si des concentrations plus élevées sont découvertes lors de tests en laboratoire, le produit doit être retiré du marché.
ONU – Convention de Stockholm pour les POP
Le Forum intergouvernemental sur la sécurité chimique (IFCS) et le Programme international sur la sécurité chimique (IPCS) ont préparé une évaluation des 12 pires substances, connues sous le nom de « sale douzaine », comme étant les premiers POP répertoriés dans les annexes de la Convention de Stockholm. Ces substances comprenaient les pesticides Aldrin, Chlordane, DDT, Dieldrin, Endrin, Heptachlore, Hexachlorobenzene HCB, Mirex, Toxaphene ; et des produits chimiques industriels, les biphényles polychlorés PCB, les dibenzo-p-dioxines polychlorées PCDD et les dibenzofuranes polychlorés PCDF.
Le CNI s’est réuni cinq fois entre juin 1998 et décembre 2000 pour élaborer la convention, et les délégués ont adopté la Convention de Stockholm sur les POP lors de la Conférence des plénipotentiaires convoquée en mai 2001 à Stockholm, en Suède. La convention est entrée en vigueur le 17 mai 2004 avec la ratification initiale de 128 parties et 151 signataires. Les cosignataires ont convenu d’interdire neuf des douze sales produits chimiques.
La première série de nouveaux produits chimiques à ajouter à la convention a été convenue lors d’une conférence à Genève le 8 mai 2009.
En 2009, l’acide perfluorooctane sulfonique et ses dérivés -PFOS- ont été inclus dans la Convention de Stockholm des Nations Unies pour éliminer leur utilisation (décision SC-4/17). En 2019, suite à l’évaluation par la POPRC-14 en 2018 au siège de la FAO à Rome du besoin continu de PFOS, de ses sels et dérivés, la COP9 a modifié l’Annexe B pour supprimer plusieurs des exemptions spécifiques et des objectifs acceptables pour le PFOS (décision SC-9/4).
• UNEP/POPS/POPRC.2/17/Add.5 : Profil de risque pour le sulfonate de perfluorooctane
• UNEP/POPS/POPRC.3/20/Add.5 : Évaluation de la gestion des risques liés au sulfonate de perfluorooctane
• UNEP/POPS/POPRC.4/15/Add.6 : Addendum à l’évaluation de la gestion des risques liés au sulfonate de perfluorooctane
En 2019, la COP9 a inscrit le PFOA et ses dérivés à l’Annexe A de la Convention de Stockholm (décision SC-9/12). Le Secrétariat du POPRC a élaboré une liste indicative de substances, contenant à l’origine environ 4 700 composés ; la liste doit être mise à jour périodiquement. Le PFOA est interdit par le règlement POP depuis le 4 juillet 2020.
• UNEP/POPS/POPRC.12/11/Add.2 : Profil de risque pour le PFOA, ses sels et les composés apparentés au PFOA.
• UNEP/POPS/POPRC.12/INF/5 : Informations supplémentaires relatives au profil de risque du PFOA, de ses sels et des composés apparentés au PFOA.
• UNEP/POPS/POPRC.13/7/Add.2 : Évaluation de la gestion des risques liés au PFOA, à ses sels et aux composés liés au PFOA.
• UNEP/POPS/POPRC.14/6/Add.2 : Addendum à l’évaluation de la gestion des risques liés au PFOA, à ses sels et aux composés liés au PFOA.
• UNEP/POPS/POPRC.17/INF/14/Rev.1 : Liste indicative mise à jour des substances couvertes par la liste du PFOA, de ses sels et des composés apparentés au PFOA.
En juin 2022, la Convention de Stockholm des Nations Unies a également décidé d’inclure le PFHxS et les composés associés dans le traité. La Commission a ajouté ce groupe de substances dans le règlement de l’UE sur les POP en mai 2023 et le règlement est entré en vigueur le 28 août 2023.
Le POPRC examine actuellement les PFCA à chaîne longue et les composés apparentés proposés pour inscription aux annexes de la Convention de Stockholm.
• UNEP/POPS/POPRC.17/7 : Proposition visant à inscrire les acides perfluorocarboxyliques à longue chaîne, leurs sels et composés apparentés dans les annexes A, B et/ou C de la Convention de Stockholm sur les polluants organiques persistants.
Livres blancs du panel d’experts IPEN PFAS 2018-2019
Trois livres blancs influents produits par le groupe d’experts de l’IPEN PFAS en 2018-2019, coordonnés par Roger Klein et ses collègues, ont été présentés au POPRC14 de la Convention de Stockholm des Nations Unies en 2018, à la COP9 et au POPRC15 en 2019 pour discuter des progrès réalisés dans la transition des mousses anti-incendie AFFF aux mousses anti-incendie F3, problèmes associés aux PFAS et PFHxS. Ces livres blancs ont aidé le Comité à parvenir à l’inscription de ces PFAS dans les annexes appropriées pour restriction ou interdiction en 2019 et 2022.
En septembre 2022, la Convention de Stockholm des Nations Unies comptait 186 parties (185 États et l’Union européenne). Les États non ratifiants notables comprennent les États-Unis, Israël et la Malaisie.
Règlement UE
Le premier produit à être réglementé a été le PFOS.
La Norvège a interdit l’utilisation de matériaux contenant du PFOS en 2007.
Le règlement de la Commission de l’Union européenne (n° 757/2010) exigeait que toute mousse contenant du PFOS au-dessus de 10 mg/kg (0,001 % p/p ou 10 ppm) ne soit pas utilisée après le 27 juin 2011 et a été adopté par l’Agence britannique pour l’environnement. en février 2011.
En janvier 2014, l’Agence norvégienne pour l’environnement a publié le règlement FOR-2013-05-27-550, qui interdit l’utilisation de l’acide perflurooctanoïque -PFOA- et de ses sels et esters.
Des limites ont été mises en œuvre le 1er juillet 2014 pour tous les produits fabriqués, importés, exportés et commercialisés en Norvège, à l’exception de certains articles spécifiques pour lesquels les nouvelles règles ont été appliquées le 1er janvier 2016.
En 2020, l’UE 2020/784 réglemente l’utilisation du PFOA et limite la teneur à 25 ppb. En théorie, il peut être utilisé jusqu’en 2025 si tous les effluents peuvent être confinés, ce qui est impossible à garantir. Dans les faits, la réglementation élimine le PFOA en Europe.
Les acides carboxyliques perfluorés à longue chaîne (PFCA en C9-14), leurs sels et leurs précurseurs sont restreints dans l’UE/EEE – Règlement UE 2021/1297 – à partir de février 2023.
L’Allemagne – soutenue par la Suède, les Pays-Bas, le Danemark et la Norvège – a proposé une restriction supplémentaire pour l’acide perfluorohexanoïque C6 -PFHxA-, ses sels et substances associées. Cette proposition est très importante car elle interdirait effectivement l’utilisation de mousses AFFF de fluorotélomères C6. Cette proposition a été évaluée par l’ECHA en décembre 2021.
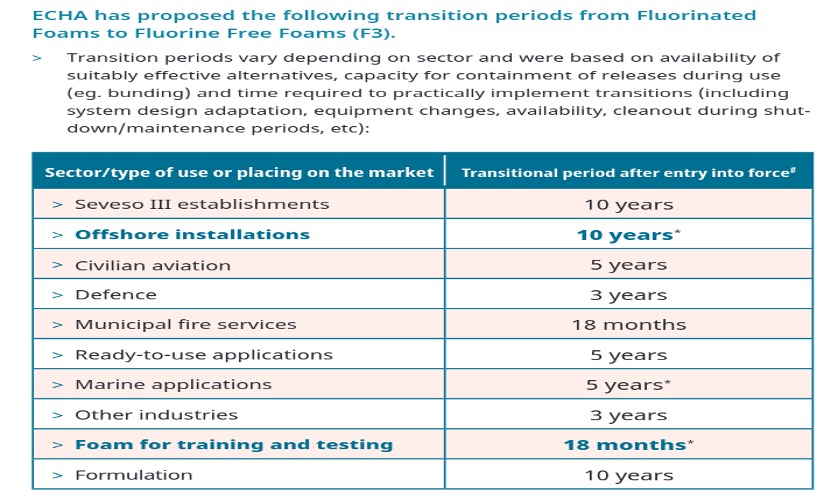
L’Agence européenne des produits chimiques -ECHA- évalue une restriction sur une interdiction des PFAS dans les mousses anti-incendie à l’échelle de l’UE. La restriction pourrait réduire les émissions de PFAS dans l’environnement d’environ 13 200 tonnes sur 30 ans [*juin 2023 ECHA/NR/23/19]. Une réponse devrait être donnée en janvier 2024.
AUSTRALIE
Jusqu’à récemment, il n’y avait pas d’approche fédérale pour réglementer l’utilisation des AFFF en Australie ; mais chaque État avait sa propre manière de restreindre l’utilisation des mousses fluorées.
Canberra – Fédéral – a publié en mai 2020 le NEMP 2.0 pour établir une base pratique pour des directives et des normes environnementales cohérentes à l’échelle nationale pour la gestion de la contamination par les PFAS. Une ébauche de restriction des PFAS dans NEMP 3.0 a été publiée en septembre 2022.
Queensland
Les pompiers du Queensland utilisent la mousse F3 depuis 2003
Les autorités environnementales du Queensland contrôlent la teneur en PFAS des produits AFFF et interdisent le PFOS.
Nouvelle Galles du Sud
Les services d’incendie utilisaient les mousses 3M ; et a arrêté leur utilisation en 2007. Le Règlement sur les opérations de protection de l’environnement 2022 interdit et restreint l’utilisation de mousse anti-incendie PFAS en Nouvelle-Galles du Sud afin de réduire son impact sur l’environnement, tout en autorisant son utilisation pour prévenir ou combattre les incendies catastrophiques par les autorités compétentes et exempter entités. Le règlement est conforme à la déclaration de position nationale sur les PFAS et constitue la première étape pour atteindre les objectifs convenus dans la déclaration.
Victoria
En 2007, le service d’incendie de Victoria – MFB – a pris la décision de remplacer la mousse anti-incendie existante par une mousse anti-incendie sans fluor. Cette décision a été prise sur la base de préoccupations liées à la santé des pompiers et aux enjeux environnementaux. MFB a élaboré une « politique d’utilisation opérationnelle de la mousse anti-incendie » qui a été formellement approuvée par l’Environmental Protection Authority (EPA), WorkSafe et la Country Fire Authority (CFA). En 2011, sur la base d’études scientifiques indépendantes sur les PFAS, qui ont identifié des liens avec divers cancers et autres problèmes de santé, MFB a effectué des essais approfondis et Fire Rescue Victoria a évalué diverses mousses anti-incendie sans fluor dans des scénarios d’incendie de liquide inflammable de classe B. MFB a constaté que la mousse sans fluor fonctionnait systématiquement bien pour éteindre les incendies de classe B et fournissait aux pompiers MFB un moyen d’extinction alternatif « plus sûr » éprouvé. Ce travail a fourni à MFB une solution opérationnelle de mousse anti-incendie qui pourrait être utilisée efficacement sur les sites du ministère de la Défense, tels que les bases aériennes de la RAAF à Point Cook et Laverton. Cela permet à MFB et FRV de répondre à leurs obligations de fourniture de services d’urgence aux bases de la Défense utilisant de la mousse anti-incendie ne contenant pas de PFAS. En 2014, tous les appareils de lutte contre l’incendie MFB avaient été convertis pour ne transporter que de la mousse de classe B sans fluor -F3- dans leurs réservoirs de mousse.
Australie du Sud
Une interdiction sur les mousses fluorées est entrée en vigueur en Australie-Sud en janvier 2018, mais les titulaires de licence ont la possibilité de demander une exemption dans certaines circonstances.
Australie occidentale
Des travaux détaillés ont été entrepris pour identifier et gérer les PFAS en décembre 2017 ; mais maintenant suivant le NEMP fédéral.
Tasmanie
TasPorts est un leader dans l’approche de la Tasmanie en matière de gestion des PFAS et a complètement éliminé toutes les mousses contenant des PFAS de l’île.
Aéroports
Depuis 2010, Airservices transporte de la mousse anti-incendie sans PFAS dans tous les aéroports civils où elle opère.
NOUVELLE ZELANDE
La Nouvelle-Zélande a exclu l’utilisation du PFOS et du PFOA dans toute substance solide ou liquide importée ou fabriquée pour être utilisée comme produit chimique de lutte contre les incendies dans la norme de 2006 du Fire Fighting Chemicals Group en vertu de la loi néo-zélandaise de 1996 sur les substances dangereuses et les nouveaux organismes.
La contamination du sol et de l’eau par les mousses anti-incendie a été réexaminée en décembre 2020. L’interdiction totale des PFAS dans les mousses anti-incendie s’appliquera à partir de décembre 2025.
Food Standards Australia & New Zealand (FSANZ) a lancé une surveillance des produits chimiques perfluorés dans les aliments depuis avril 2017, avec des directives sanitaires pour les valeurs de dose d’apport quotidien pour le PFOS, le PFOA et le PFHxS.
CANADA
Le Canada a toujours été à l’avant-garde de la sensibilisation et de la réglementation en ce qui concerne les risques inhérents et potentiels liés au rejet de PFAS dans l’environnement et à l’exposition de la population humaine à la contamination par les PFAS par l’eau potable, les produits agricoles et l’usage domestique.
Le gouvernement du Canada envisage des règles qui traiteraient les PFAS en tant que classe plutôt qu’en tant que substances individuelles ou en groupes plus petits. Aborder les PFAS en tant que classe de produits chimiques réduirait les risques de substitution regrettable, soutiendrait des programmes de recherche et de surveillance plus holistiques et offrirait la possibilité de réduire l’exposition future de l’environnement et des humains aux PFAS. Un avis d’intention concernant la vaste catégorie de PFAS a été publié dans la Gazette du Canada, Partie I : Vol. 155 n°17 – 24 avril 2021.
En réponse à l’engagement décrit dans l’avis d’intention, le gouvernement du Canada a publié un projet de rapport sur l’état des substances per- et polyfluoroalkylées (PFAS) pour consultation publique pendant 60 jours. L’avis connexe a été publié dans la Gazette du Canada, Partie I : Vol. 157, n° 20 – 20 mai 2023.
Actuellement, seul un nombre limité de sous-groupes de PFAS sont soumis à une réglementation au Canada. Le PFOS, le PFOA, les PFCA-LC et leurs dérivés connexes ont été évalués et ajoutés à la liste des substances toxiques en vertu de l’annexe 1 de la Loi canadienne sur la protection de l’environnement (1999) (LCPE).
USA
En 2004, on estimait qu’il y avait environ 45 millions de litres de concentré AFFF aux États-Unis et dans leurs territoires.
La National Defense Authorization Act, adoptée par le Congrès fin 2019, exigeait que la marine américaine publie une nouvelle spécification militaire pour une mousse sans fluor d’ici fin janvier 2023 et exigeait une transition complète vers des mousses anti-incendie sans fluor d’ici octobre 2024. IL avait imposé à la FAA des mandats pour faire passer les aéroports à des mousses sans fluor d’ici octobre 2021, mais cette date limite n’a pas été respectée. Les nouvelles réglementations MIL-SPEC ouvrent la voie à la transition des aéroports et des bases militaires de la FAA, nécessitant des investissements importants. Selon un rapport du Congrès de 2021, les aéroports militaires et civils disposent encore d’environ 50 millions de litres de concentré AFFF dans leurs installations. Bien que l’armée n’ait pas encore officiellement approuvé une mousse sans fluor à utiliser dans ses installations, il existerait désormais un petit nombre de produits disponibles dans le commerce qui ont passé avec succès les tests de performance appropriés tels que UL.
Aux États-Unis, chaque État suit sa propre voie. Le scandale de la non-divulgation d’informations sur la toxicité des produits fluorés et l’impact environnemental, ainsi que d’informations purement erronées, est né d’une longue série de procès contre les fabricants de matières premières PFAS. L’histoire a même culminé avec la publication d’annonces d’avocats à la recherche de clients pour saisir le tribunal !

Les gouvernements des États prennent des mesures législatives et réglementaires pour éliminer progressivement les PFAS des produits afin de prévenir la contamination au profit d’alternatives plus sûres. Par exemple, les lois du ME et de WA ont donné aux agences d’État le pouvoir d’interdire les PFAS dans une large gamme de produits. La loi du Maine oblige les fabricants de produits à divulguer la présence de PFAS. Plusieurs États ont adopté des restrictions sur les PFAS dans les textiles, l’État de Californie interdisant les PFAS dans presque tous les textiles d’ici 2025, et l’État de New York les limitant dans les vêtements, l’État de Washington les interdisant dans les meubles rembourrés et l’État de Washington allant de l’avant avec des mesures réglementaires sur de nombreuses catégories de produits textiles. Six États (CA, CO, ME, MD, NY et VT) ont adopté des restrictions sur les PFAS dans les tapis, les moquettes et les traitements textiles après-vente. Douze États (CA, CO, CT, HI, MD, ME, MN, NY, OR, RI, VT et WA) ont promulgué des interdictions étatiques sur les PFAS dans les emballages alimentaires. Quatre États (CA, CO, MD et WA) ont adopté des restrictions sur les PFAS dans les produits de soins personnels. CO a également adopté des restrictions sur les produits pétroliers et gaziers. Onze États, dont CA, CO, CT, HI, IL, ME, MD, NH, NY, VT et WA, ont mis en place des interdictions sur la vente de mousse anti-incendie contenant des PFAS. Avec la législation adoptée l’année dernière, WA évalue des alternatives plus sûres aux PFAS dans d’autres produits tels que les vêtements, les nettoyants, les revêtements et les finitions de sol, les équipements de pompier et autres, avec un calendrier d’adoption de restrictions d’ici 2025. Source www.saferstates.org
Sous la pression et la menace financière des procès judiciaires, la plupart des fabricants américains ont arrêté la fabrication des émulseurs AFFF et ont lancé la promotion des produits sans fluor, non seulement aux USA, mais aussi auprès de leurs marchés et clients traditionnels à l’international.
Élimination des déchets PFAS
Il s’agit d’un problème énorme et potentiellement extrêmement coûteux. Lors d’incidents majeurs tels que Milford Haven (août 1983), Sandoz Basel (novembre 1986), Coode Island (Melbourne août 1991), Buncefield (décembre 2005) ou Campbellfield (Melbourne avril 2019), des dizaines de millions de litres contaminés par les eaux de ruissellement des eaux d’incendie ont été rejetés dans l’environnement – le confinement total lors d’incidents aussi importants est presque impossible et tous les déchets collectés doivent être éliminés de manière appropriée. Les anciens stocks d’émulseurs fluorés représentent une dépense financière importante dans le cadre de la transition vers des produits sans fluor, tout comme la décontamination des équipements fixes et mobiles.
Actuellement, la méthode la plus efficace, la plus réalisable financièrement et la plus durable sur le plan environnemental pour éliminer de grandes quantités de déchets solides ou liquides contaminés par les PFAS semble être l’incinération à très haute température. Les coûts peuvent varier entre 1 000 et 3 000 USD par tonne, en fonction du niveau accepté de contaminant fluoré résiduel.
CONCLUSION
De plus en plus de réglementations, notamment en Europe et en Australie/Nouvelle-Zélande, ciblent les applications particulièrement dispersives utilisant des PFAS telles que les mousses anti-incendie. La transition des mousses AFFF aux mousses sans fluor -F3- est devenue possible, compte tenu des progrès technologiques rapides au cours des 5 à 10 dernières années et des produits sans fluor capables de rivaliser avec les AFFF sur la base de leurs performances.
De nombreuses grandes organisations telles que les aérodromes civils et militaires, ainsi que les industries pétrolière et gazière, chimique et mécanique telles que Equinor, Bayer, Lufthansa et BMW, sont déjà devenues sans fluor, ayant également résolu les problèmes de décontamination des équipements contaminés par les AFFF. ainsi que la compatibilité en termes de systèmes de livraison et de formation opérationnelle.
Plus récemment, nous avons constaté une certaine prise de conscience au sein des organismes de réglementation de l’environnement – Singapour, Mexique, Colombie – démontrant un profond intérêt pour ce qui se passe dans d’autres pays ; il est probable que l’interdiction des « produits chimiques éternels » soit étendue à la communauté mondiale dans les 5 à 10 prochaines années !
References
Krogerus, M. (2012) The Decision Book: Fifty Models for Strategic Thinking. Tschäppeler, R. and Piening, J. (1st American edition), New York, W.W. Norton & Co., pp. 86-87.
Rumsfeld, D. (2002)
Rio Convention (1992)
United States (1933) Securities Act.
Preston, B.J. (2017) The Judicial Development of the Precautionary Principle. Queensland Government Environmental Management of Firefighting Foam Policy Implementation Seminar 21 February 2017, Brisbane, Qld., pp. 26.
Preston, B.J. (2018) ‘The Judicial Development of the Precautionary Principle’ Environmental and Planning Law Journal 135, 23-42.
Allcorn, M., T. Bluteau, J. Corfield, G. Day, M. Cornelsen, N.J.C. Holmes, R.A. Klein, J.G. McDowall, K.T. Olsen, N. Ramsden, I. Ross, T.H. Schaefer, R. Weber, K. Whitehead. (2018) “Fluorine-Free Firefighting Foams (3F) Viable Alternatives to Fluorinated Aqueous Film-Forming Foams (AFFF).” UN Stockholm Convention POPRC14 Rome 17-21 September 2018, IPEN Gothenburg Sweden: IPEN F3 Expert Panel. < www.ipen.org >
Bluteau, T., M. Cornelsen, G. Day, N.J.C. Holmes, R.A. Klein, J.G. McDowall, K.T. Olsen, M. Tisbury, and L. Ystanes. (2019) “The global pfas problem: fluorine-free alternatives as solutions firefighting foams and other sources-going fluorine-free.” UN Stockhom Convention COP9 Geneva Apr-May 2019, IPEN Gothenburg Sweden: IPEN F3 Expert Panel. < www.ipen.org >
Bluteau, T., M. Cornelsen, N.J.C. Holmes, R.A. Klein, M. Tisbury, and K. Whitehead. (2019) “Perfluorohexane sulfonate (pfhxs)-socio-economic impact, exposure, and the precautionary principle.” UN Stockholm Convention POPRC15 Rome Sep-Oct 2019, IPEN Gothenburg Sweden: IPEN F3 Expert Panel.
< www.ipen.org >
3F AMERICAS A VU LA LUMIERE
3F AMERICAS va démarrer la promotion et la distribution d’un ensemble de nouveaux produits grâce à son réseau de distribution en Amérique Latine. Ces nouveaux produits sont une véritable révolution dans le domaine de la protection individuelle des pompiers.
Un des équipements est un ligne guide lumineuse qui fonctionne dans les 2 sens. La ligne résiste à la chaleur, à l’abrasion et est déclinée en 3 versions : une ligne personnelle de 25 mètres, une ligne portable de 50 mètres, et une ligne waterproof de 25 mètres pour les opérations aquatiques.
L’autre équipement est un avertisseur de détresse personnel. Il offre plusieurs avantages UNIQUES. Il intègre 6 fonctions différentes, et génère une alarme sonore – 98 dB – et visuelle en réagissant aux mouvements, à la température et aux chocs. Il est protégé IP68 et sa batterie fonctionne 20 heures et peut être rechargée directement sur son socle de chargement. C’est le plus léger du marché avec un poids de 120 g. En savoir plus…
