Des AFFF aux F3 : Chimie – Partie 2
Dans cette partie, nous traitons de la chimie impliquée dans la formulation de mousses de classe A pour les combustibles carbonés, et des mousses AFFF de classe B basées sur la chimie du PFOS pour les incendies d’hydrocarbures liquides et de solvants polaires.
Dans la première partie de cette série d’articles, nous avons vu que les mousses anti-incendie AFFF contiennent diverses substances perfluoroalkyl (PFAS); cependant, la mousse anti-incendie n’est qu’une des nombreuses applications des PFAS.
Les PFAS sont utilisés depuis des décennies dans plus de 200 autres applications industrielles et domestiques, telles que l’emballage alimentaire, le traitement du cuir et des textiles, la protection antitaches des tapis et des vêtements, les détergents, l’imperméabilisation à l’eau et à l’huile, les peintures et les vernis, les encres d’imprimerie, le chromage, les vêtements d’extérieur et de protection (EPI) pour les services d’urgence et militaires. Ces substances perfluorées sont largement utilisées car elles offrent une combinaison de propriétés uniques, y compris la capacité de repousser l’eau (hydrophobie), la capacité de repousser les huiles (oléophobie), la capacité de réduire la tension superficielle des solutions aqueuses à moins de 20 dynes/cm et avec elle agissant comme détergents, émulsifiants, agents mouillants et dispersants.
L’OCDE (2021) a récemment clarifié la définition de ce qui constitue un PFAS, tout en reconnaissant, selon Buck et coll. (2011), les éléments suivants :
« Les PFAS sont définies comme des substances fluorées s’ils contiennent au moins un atome perfluoré de carbone de méthyle ou de méthylène (sans atome H/Cl/Br/I attaché à celui-ci),c’est-à-dire, à quelques exceptions près, que tout produit chimique ayant au moins un groupement méthyle perfluoré (–CF3) ou un
groupement méthylène perfluoré (–CF2–) est un PFAS. »
Plus de 800 produits actuellement disponibles sur le marché ont été identifiés, mais la véritable liste des PFAS utilisés dans le commerce et l’industrie est susceptible d’être de 10000 ou plus; la Convention de Stockholm des Nations Unies a répertorié 4700 substances liées au PFOA seul. Les PFAS ont commencé à être fabriqués en grandes quantités au début des années 50. Tous sont anthropiques créés par l’homme à l’aide de la synthèse chimique et ils n’existent pas naturellement. Les produits finaux perfluorés extrêmement stables, résistants aux produits chimiques et à la dégradation dans l’environnement ont longtemps été identifiés comme des « produits chimiques éternels », par exemple par des scientifiques et des journalistes comme Rebecca Renner [« Growing Concern Over Perfluorinated Chemicals » (2001) Environ. Sci. Technol. 35(7) 154A-160A; « The long and the short of perfluorinated replacements » (2006) Environ. Sci. Technol. 40(1) 12-13] or Sharon Lerner writing in the Intercept [« Toxic Chemicals Discovered in Hundreds of Products » Sharon Lerner (The Intercept, décembre 2020)].
Il faut souligner que, bien que les PFAS soient encore communément et incorrectement appelés ‘’contaminants émergents’’, ils sont vraiment devenus des contaminants préoccupants depuis au moins 10 ans et ne devraient plus être qualifiées de ‘’nouveaux’’. D’autre part, la technologie pour traiter les résidus de PFAS est actuellement encore émergente et en développement.
Les mousses anti-incendie sont dites de classe A pour les feux de combustibles carbonés tels que le bois, le papier ou la végétation, agissant comme agents mouillants améliorant la pénétration de l’eau dans les incendies en profondeur et ne contiennent pas de tensioactifs fluorés, seulement des tensioactifs dhydrocarbonés; ou, d’autre part, les mousses de classe B sont spécifiquement formulées pour les hydrocarbures liquides tels que l’essence et les solvants polaires tels que l’éthanol. Les mousses modernes de classe B peuvent contenir soit des tensioactifs fluorés et être capables de formation de film à l’interface air-carburant (AFFF), soit des mousses F3 sans fluor, spécialement formulées contenant uniquement des tensioactifs hydrocarbonés. Il est intéressant de noter que les mousses sans fluor de classe B (F3) peuvent être utilisées efficacement pour les feux de classe A et de classe B, contrairement aux AFFF.
Additifs de classe A pour combustibles carbonés
Les mousses anti-incendie de classe A sont largement utilisées dans le monde entier, en particulier en Australie, en Amérique du Nord et en Europe du Sud, pour les incidents impliquant des combustibles carbonés, par exemple les incendies de bâtiments, les dépôts de plastique et de pneus, ainsi que les prairies et les feux de forêts. Ted Schaefer ,travaillant alors pour 3M Australie à la fin des années 1980, a mis au point l’une des premières mousses efficaces de classe A, ‘’3M Fire-Brake BFFF’’, reconnue en 2001 par l’Académie australienne des sciences technologiques et de l’ingénierie comme l’une des 100 meilleures inventions australiennes du XXe siècle.
Les mousses de classe A se comportent très différemment des AFFF contenant des tensioactifs fluorés, car elles sont spécifiquement formulées pour pénétrer efficacement les combustibles carbonés, tels que la végétation compactée, le papier ou le bois, en utilisant des tensioactifs hydrocarbonés spéciaux, peu différents à voir avec un détergent ménager. Les AFFF avec tensioactifs fluorés, conçus pour l’application en surface sur des incendies d’hydrocarbures liquides ou de solvants polaires, sont loin d’être aussi efficaces pour pénétrer aussi profondément les substrats solides. Il est franchement trompeur d’entendre certains membres de l’industrie affirmer que leurs produits AFFF peuvent être utilisés comme émulseurs de classe A et de classe B.


Mister H: Pénétration avec du Classe A. Mister F: Impossibilité à pénétrer avec du Classe B AFFF
(Bluteau 2007)
Le comportement différent d’un additif de classe A à base de tensioactifs hydrocarbonés et d’un AFFF fluoré de classe B vis-à-vis d’un combustible carboné peut être mis en scène dans ce dessin utilisé pour la première fois par l’un d’entre nous en 2007. Mister H, une véritable mousse de classe A peut pénétrer dans le carburant carboné en raison de ses caractéristiques de mouillage optimisées ; Mister F, un tensioactif fluoré de base d’AFFF, ne peut pas pénétrer en raison de ses propriétés hydrophobes et oléophobes.
Emulseur AFFF de classe B pour hydrocarbures liquides et solvants polaires
Le premier rapport sur une mousse AFFF, appelée LightWater®, par R.L. Tuve et al, du Laboratoire de recherche navale et de la société 3M, en mars 1964, fait état d’une mousse capable d’éliminer l’évaporation et de former un film à la surface de combustibles inflammables à bas point d’éclair tels que l’essence, et démontre qu’il est 1200% plus efficace que les mousses protéiniques standard dans des conditions identiques.
Les composés utilisés dans les formulations d’émulseurs de 3M appartenaient à la classe générale des dérivés de l’acide perfluorosulfonique, certains étant des sels quaternaires, d’autres étant des alcools, des esters, des sels anioniques d’acides sulfonamido carboxyliques substitués, etc. Tous ces composés sont hydrosolubles, Les fluorocarbures de poids moléculaire élevé ont montré un abaissement de la tension superficielle de l’eau à moins de 20 dynes/cm. En général, ils sont insensibles aux électrolytes et montrent une activité superficielle lorsqu’ils sont dissous dans des solvants organiques.
Le premier brevet pour un AFFF a été accordé à Richard Tuve et Edwin Jablonski en juin 1966 [1], représentant une nouvelle ère dans les émulseurs de lutte contre les incendies qui devait durer 30 à 40 ans jusqu’à ce que la 3M Company Minnesota se retire complètement de la chimie à base de PFOS en mai 2000.
Les informations de la littérature existante dans les brevets donnent un aperçu fascinant des dérivés utilisés dans ces premiers AFFF. Des dérivés du perfluorooctane sulfonamide (PFOSA) et de l’acide perfluorooctane carboxylique (PFOA) ont été utilisés. Comme l’indique le brevet de 1966, ces premières formulations comprennent les sels d’ammonium quaternaire du PFOS et des dérivés amido du PFOA :
C8F17-SO2NH2-(CH3)3N(CH3)3+I–
C7F15-CONH-(CH3)3N(CH3)3+I–
un dérivé amphotère du PFOA à base d’aminobétaïne
C7F15-CONH-(CH2)3–N+(CH3)2-CH2-CH2-COO–
et le sel de potassium d’un dérivé sulfamide de PFOS
C8F17SO2N(C2H5)-CH2COOK
Le sel de potassium du PFOS sous forme de tensioactif FC-95 a également été utilisé dans les premiers émulseurs.
Il est intéressant de noter que quelques 50 ans plus tard, Barzen-Hanson et al en 2017 [2] du groupe de Jennifer Field à l’Université d’État de l’Oregon a identifié une vaste gamme d’autres dérivés, ou leurs produits de décomposition, impliquant 40 classes différentes dans les anciens AFFF.
Fluoration électrochimique (ECF) – le procédé Simons
La société 3M a annoncé en mai 2000 qu’elle éliminait progressivement la production de tensioactifs fluorés sur base de PFOS et qu’elle se retirait entièrement du marché des émulseurs AFFF, ce qui marquait la fin de la disponibilité des produits Light Water™ et Light Water™ ATC™ (3M Company (2000)). Parmi les autres produits utilisant le PFOS, mentionnons les traitements antitaches ScotchGuard et hydrofuges. On pense que la production de PFOS par la société 3M a complètement cessé vers 2002, étant remplacée par le composé à chaîne plus courte PFBS – C4-, alors que la production de PFOS et de PFHxS se soit poursuivie depuis en Chine et en Inde.
Jusqu’en 2000, le PFOS était fabriqué selon le procédé de fluoration électrochimique ECF de Simons (3M Company, 1999; Ignat’ev et coll., 2009; Sartori et Ignat’ev, 1998). Ce procédé consiste à remplacer les atomes d’hydrogène de l’octyl sulfonate par l’utilisation électrolytique du fluorure d’hydrogène afin de produire du fluorure de perfluorooctane sulfonyle, le PFOSF.
C8H17SO3H + HF ==>> C8F17(C=O)F
Le PFOSF est un fluorure d’acyle hautement réactif qui sert de base à la préparation de dérivés du PFOS comme le sulfonamide PFOSA ou le N-éthyl-PFOSA, par exemple :
C8F17(C=O)F + C2H5NH2 ==>> C8F17(C=O)-NH-C2H5
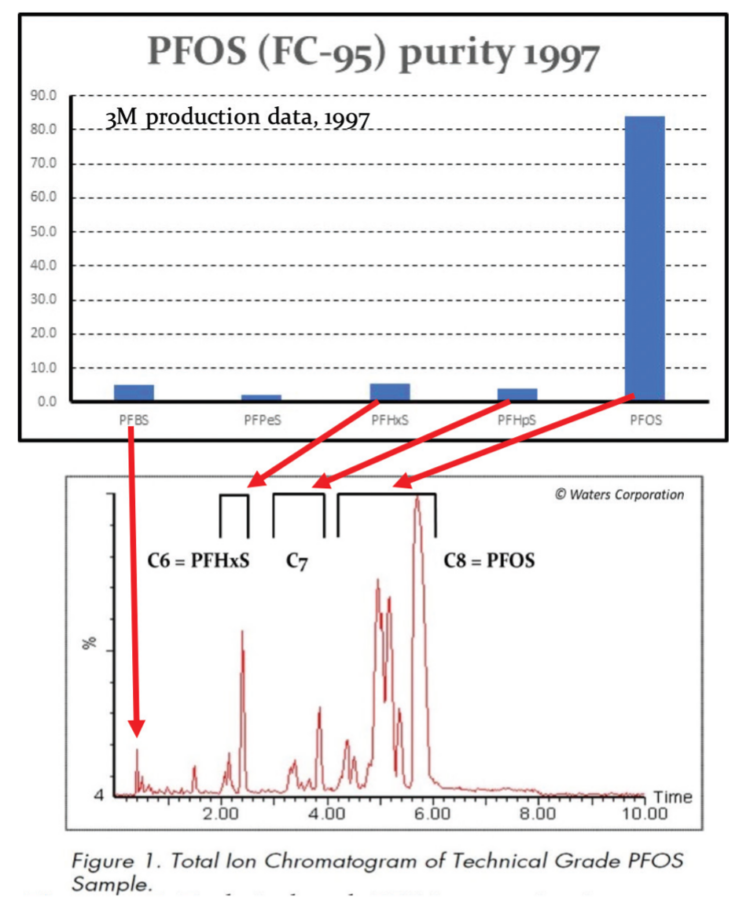
La production de PFOSF à l’aide de la fluoration électrochimique ECF était, et demeure, un procédé intrinsèquement ‘’sale’’ qui a donné lieu à une vaste gamme d’isomères structuraux, à chaîne droite et ramifiés avec CF-CF3 et C-(CF3).2 chaînes latérales, ainsi que des homologues de longueur de chaîne impaire et uniforme tels que C4 PFBS, C6 PFHxS et C7 PFHpS. Par conséquent, le PFOS de qualité technique a toujours été et continue d’être contaminé par un pourcentage important de PFHxS. De plus, les chaînes perfluoroalkyles du PFOS et du PFHxS peuvent former des hélices gauches ou droites qui donnent des pseudo-racémates qui ont été détectées dans les sérums humains (Wang et al., 2011; Naile et al., 2016; Sasaki et al., 2018).
Citation de la proposition de restriction du PFHxS par l’ECHA (13 juin 2019) :
« … Des sources indiquent que lors de la fabrication de composés perfluorés, un mélange de composés de longueur de chaîne variable se forme habituellement, avec des quantités typiques de PFHxS formées lors de la fabrication de PFOS se situant entre 4 et 14 % (BiPRO, 2018) citant (Ren, 2016). Ces chiffres sont étayés par les mesures de PFHxS dans les produits commerciaux à base de PFOS, à savoir de 3,5 % à 9,8 % dans le FC-95 de 3M (BiPRO, 2018) citant 3M (2015) et de 11,2 % à 14,2 % dans trois produits de Chine (Jiang et al, 2015). La BiPRO note toutefois que la quantité de composant C6 peut être réduite par la purification à différents stades de la chaîne de production… »
L’utilisation du procédé ECF pour produire des acides sulfoniques et carboxyliques perfluorés, tels que les PFOS et PFOA et leurs dérivés, a été résumée par Buck et al [2011], comme indiqué ci-dessous.
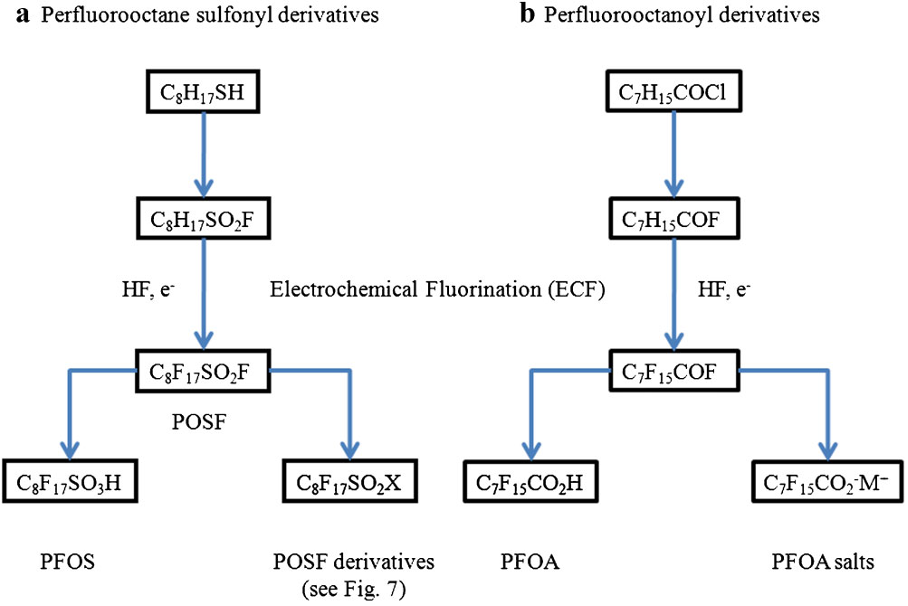
source: Buck et al (2011)
A suivre dans la partie 3.
Références
Barzen-Hanson, K.A., Roberts, S.C., Choyke, S., Oetjen, K., McAlees, A., Riddell, N., McCrindle, R., Ferguson, P.L., Higgins, C.P., and Field, J.A.. (2017) “Discovery of 40 Classes of Per- and Polyfluoroalkyl Substances in Historical Aqueous Film-Forming Foams (AFFFs) and AFFF-Impacted Groundwater” Environ, Sci. Technol. 51, 2047-2057.
Benskin J.P., De Silva A.O., Martin J.W. (2010) Isomer Profiling of Perfluorinated Substances as a Tool for Source Tracking: A Review of Early Findings and Future Applications. Rev. Environ. Contam. Toxicol.:111-160.
Buck, R.C., Franklin, J., Berger, U., Conder, J.M., Cousins, I.T., de Voogt, P., Jensen, A.A., Kannan, K., Mabury, S.A., and van Leeuwen, S.P.J. (2011) Perfluoroalkyl and polyfluoroalkyl substances in the environment: terminology, classification, and origins. Integr. Environ. Assess. Manag. 7(4), 513-541.
Ignat’ev, N.V., Willner, W., and Sartori, P. (2009) Electrochemical fluorination (Simons process) – A powerful tool for the preparation of new conducting salts, ionic liquids and strong Brǿnsted acids. J. Fluorine Chem. 130(12), 1183-1191.
Naile, J., Garrison, A.W., Avants, J.K., and Washington, J.W. Isomers/Enantiomers of Perfluorcarboxylic Acids: Method Development and Detection in Environmental Samples. Chemosphere 44, 1722-1728.
OECD (2021), Reconciling Terminology of the Universe of Per- and Polyfluoroalkyl Substances:
Recommendations and Practical Guidance, OECD Series on Risk Management, No. 61, OECD
Publishing, Paris.
Sartori, P. and Ignat’ev, N.V. (1988) The actual state of our knowledge about mechanism of electrochemical fluorination in anhydrous hydrogen fluoride. J. Fluorine Chem. 87(2(, 157-162.
Sasaki, T., Egami, A., Yajima, T., Uekusa, H., and Sato, H. (2018) Unusual Molecular and Supramolecular Structures of Chiral Low Molecular Weight Organochelators with Long Perfluoroalkyl Chains. Crystal Growth and Design 18(7) 4200-4205.
Tuve, R.L. amd Jablonksi, E.J. (1966) US 3,258,423 Patent June 28, 1966 “Method Of Extinguishing Liquid Hydrocarbon Fires”, assignors to the United States of America as represented by the Secretary of the Navy. Filed Sept. 4, 1963, Ser. No. 306,665.
Vyas, S.M., Kania-Korwel, I., Lehmler, H.J. (2007) Differences in isomer composition of perfluorooctanoylsulfonyl (PFOS) derivatives. J. Environ. Sci. Health and Toxic Hazard Substance Environ. Eng. 42, 249-255.
Wang, Y., Beeson, S., Benskin, J.P., De Silva, A.O., Genuis, S.J., and Martin J.W. (2011) Enantiomer Fractions of Chiral Perfluoroctanesulfonate (PFOS) in Human Sera. Environ. Sci. Technol. 45(20) 8907-8914
